近日,中国科学院苏州生物医学工程技术研究所郭振研究员、周连群研究员团队在ACS Applied Materials & Interfaces上发表题为“Revealing the Binding Events of Single Proteins on Exosomes Using Nanocavity Antennas beyond Zero-Mode Waveguides”的封面文章,报道了一种超越零模波导纳米光学腔,揭示外泌体表面单个蛋白质分子相互作用过程。

图1. ACS Applied Materials & Interfaces,2023, Volume 15,Number 42封面图片
研究外泌体膜表面单分子相互作用具重要的生物学意义。然而,因外泌体尺寸小,通常在几十纳米至数百纳米之间,造成检测外泌体和纳米量级蛋白的生物分子之间的结合事件是极其困难的。因此,科研人员提出了一种超越零模波导纳米光学腔,更高效激发单分子荧光,获得高的信噪比(19.5),良好的占有率(12%-23%),克服了大体积生物材料加载的纳米腔尺寸限制。
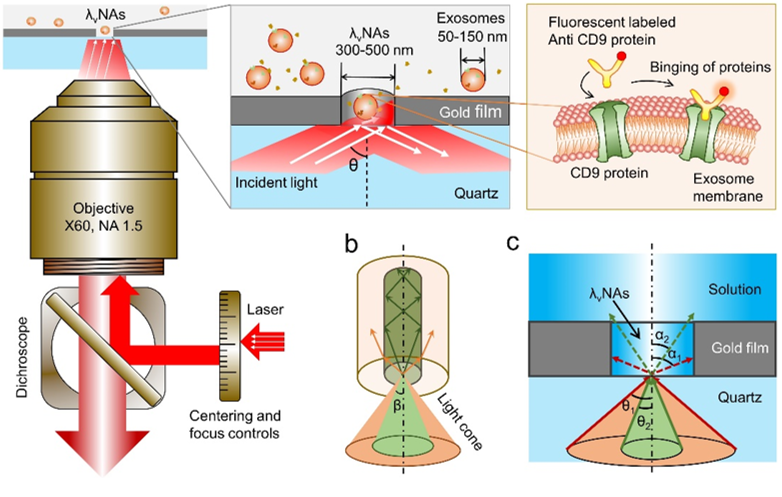
图2. 超越零模波导纳米光学腔的工作原理示意图。(a)纳米光学腔的光学检测系统示意图;(b)传统光波导的原理示意图;(c)纳米光学腔的原理示意图。
随后,科研人员进一步探索了超越零模波导纳米光学腔对外泌体表面蛋白质结合事件的动态成像。利用该方法,测量出了外泌体表面的单个跨膜CD9蛋白与其单克隆抗体之间的结合事件,表明探测单分子事件的范围突破了零模波导孔的物理尺寸的限制,可用于分析从几十纳米到数百纳米的单个分子与生物材料的相互作用,如微囊泡和凋亡体等。该研究工作为理解外泌体表面分子的相互作用提供了方法,有望应用于外泌体作用机制研究、药物筛选、肿瘤诊疗等场景。
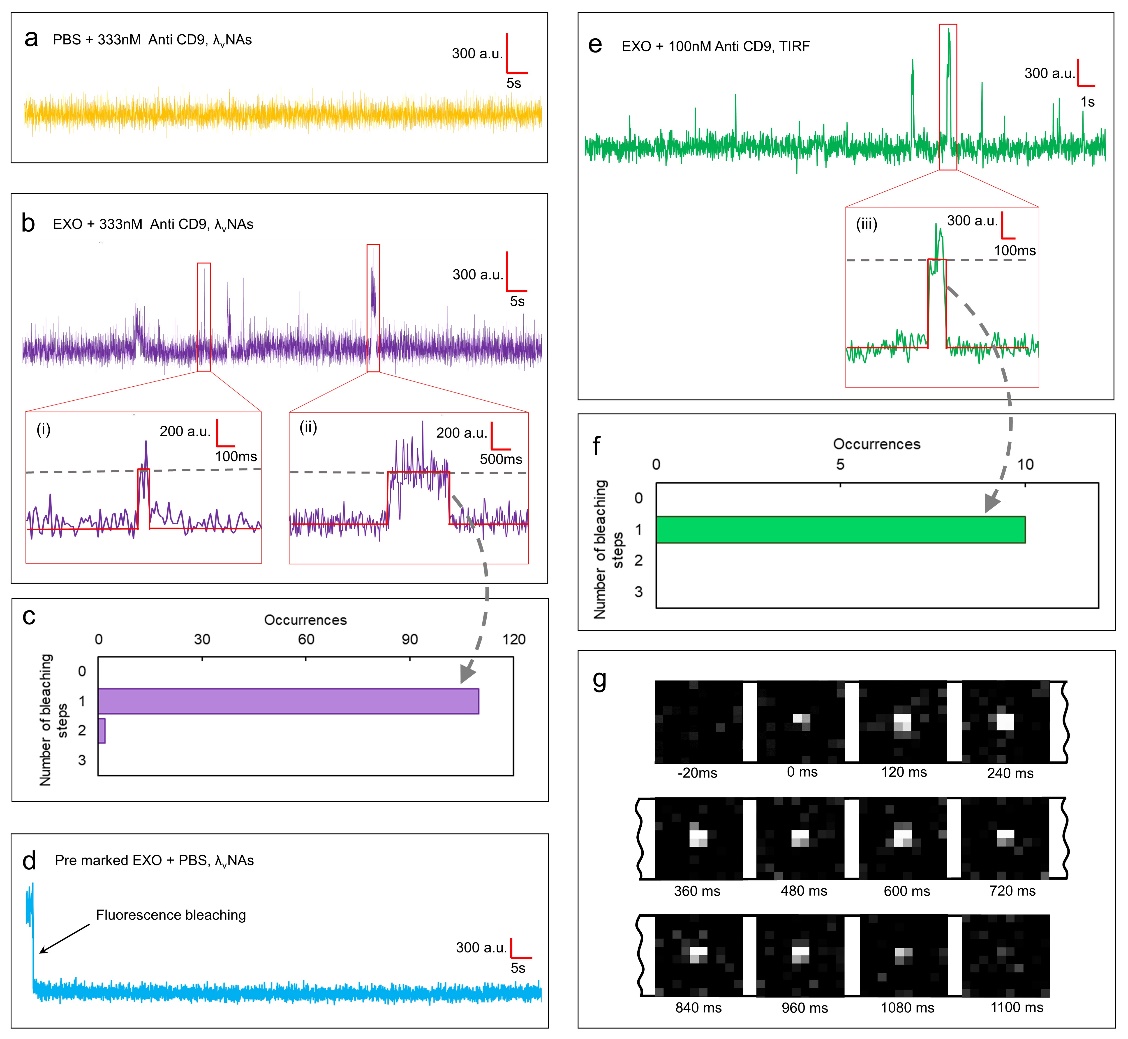
图3. 外泌体表面单个蛋白质分子结合过程中荧光信号强度的实时记录。(a、d)对照组的荧光信号实时记录结果;(b)实验组的荧光信号实时记录结果;(c)对实验组的荧光漂白步骤统计;(e)传统显微方法获得的荧光信号实时记录结果;(f)对传统显微方法的荧光漂白步骤统计;(g)单个纳米光学腔内荧光随时间变化过程的影像照片。
中国科学院苏州生物医学工程技术研究所博士研究生高庆学为本文第一作者,周连群研究员、郭振研究员为论文通讯作者。该项研究工作得到国家重点研发计划、国家自然科学基金等项目资助。
 附件下载:
附件下载: