原发性肝细胞癌(hepatocellular carcinoma,HCC)是世界常见的恶性肿瘤之一,致死率位居第二。其中微血管侵犯(microvascular invasion,MVI)是HCC具有侵袭性生物学行为的标志,被证实是HCC复发风险的重要预测指标,MVI状态关系到患者治疗方案的选择以及预后,而临床针对MVI诊断只能依靠术后组织病理学检查。目前MVI的研究热点就是术前MVI精准预测,这将有助于指导外科手术(例如术式、切缘确定)和辅助治疗(例如是否需要局部放化疗等),实现个性化治疗。
影像组学方法通过从医学影像中提取高通量信息进行深层挖掘分析,能够实现肿瘤的无创诊断和预后预测。现有影像组学方法主要集中关注肿瘤内部区域,忽略了肿瘤周围组织。病理学上,肿瘤周围组织是最先受MVI影响的区域。因此,与肿瘤区域相比,肿瘤周围组织的影像学特征可能与MVI更相关。与高分辨率的CT或MRI相比,超声检查具有操作简单、无创便携等特点,是临床上肝脏影像学检查首选检查方式。因此构建基于超声影像的HCC患者MVI状态预测模型对最佳治疗方案的制定具有重要临床意义。
中国科学院苏州生物医学工程技术研究所高欣团队与复旦大学附属中山医院超声科王文平团队合作,提出了一种基于传统灰阶超声的HCC MVI状态术前预测模型,且首次建立对MVI阳性中两种亚型M1和M2分类模型,实现对原发性肝细胞癌患者MVI状态的全面无创预测。该研究搜集九台不同型号超声设备采集的322名患者(其中178名MVI阴性患者,102名M1患者,42名M2患者)的超声影像数据及临床资料。在单幅肿瘤切面超声图像中,分别从肿瘤区域(GTR)和瘤周区域(PTR)提取高通量影像特征(图1),通过机器学习方法筛选特征并构建模型,最后使用ROC曲线下面积AUC来评估模型的分类能力。
研究结果显示,MVI阴阳性的预测任务,基于瘤周区域构建的机器学习模型较基于肿瘤区域构建的模型具有更好的预测能力(准确度为71% VS 70.8%),这也从另一角度验证了瘤周组织的影像学特征与MVI更相关。随着整合肿瘤区域及临床甲胎蛋白(AFP)指标,MVI阴阳性预测精度分别得到进一步提升(准确度分别提升了1.6%和3.4%),这表明结合影像和临床指标可获得更好的预测能力。而针对MVI阳性的亚型分类(M1和M2),相比于瘤周区域,肿瘤区域构建的机器学模型预测能力更优(准确度达到80.6%)。以上指标见表1。
本研究的意义在于,验证了以往临床忽略的瘤周区域对MVI预测的重要价值,且首次基于超声对MVI阳性中的M1和M2进行了分类预测,并结合临床征象全面客观的预测MVI状态,有望在临床中辅助医生进行HCC患者MVI状态术前精准无创诊断,为术前MVI预测提供一种新思路和新方法。
该研究受国家自然科学基金委等机构资助,相关成果Preoperative prediction of microvascular invasion in hepatocellular carcinoma: initial application of a radiomic algorithm based on grayscale ultrasound images发表于Frontiers in Oncology (doi: 10.3389/fonc.2020.00353)。其中董怡和周榴并列第一作者。
论文链接:https://www.frontiersin.org/articles/10.3389/fonc.2020.00353/full
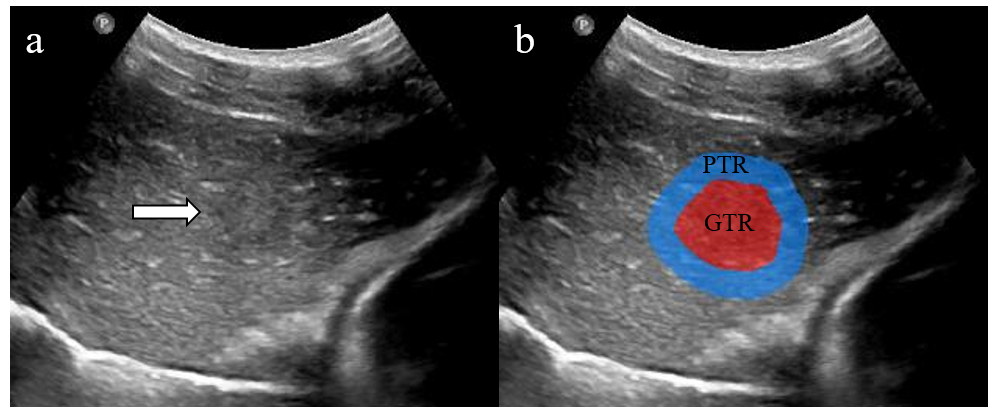
图1. 灰阶超声肿瘤切面中(a)肿瘤(GTR)与(b)瘤周区域(PTR),以及全肿瘤区域(GPTR=GTR+PTR)
表1. 各模型的MVI预测准确度。

 附件下载:
附件下载: