近年来,我国肿瘤发病率明显上升,恶性肿瘤位于我国城市居民主要疾病死亡率首位。肿瘤防治工作具有重大社会意义与科学价值,肿瘤疗效与预后评估是其中的关键研究领域。肿瘤标记物是肿瘤发生发展以及疗效好坏的重要指标,在肿瘤疗效与预后评估中起着至关重要的作用,如何找出有效的肿瘤标记物是当前研究的重要挑战。
随着分子技术的发展,特别是下一代基因测序技术的发展,通过基因或蛋白质分子技术,从癌症的分子机制去探索其发生的根源,寻找致癌基因的突变位点和癌症基因的分子表达通路,获取分子标记物,已成为当前肿瘤标记物研究的主流。其突出特点是生物分子层次的解释性强,但获取上述分子标记物的费用及技术门槛高,需借助手术或穿刺活检侵入性采样,只能单点单次采集,无法全面描述肿瘤组织的时间与空间异质性。
随着医学影像技术的快速发展,通过医学影像可无创、实时、可重复地获取肿瘤全局形态与分子功能信息,借助模式识别、机器学习等图像分析手段,构建与预后或疗效显著相关的肿瘤影像标记物。通过影像标记物,我们可对肿瘤进行早期诊断,并能在治疗过程中随时跟踪肿瘤的发展情况。但影像标记物可解释性不强,尤其是缺乏潜在的生物和分子机制的解释。
开展肿瘤影像基因组学研究,结合影像学和基因组学各自优势,探索影像标记物与分子标记物的关联,可将分子层次信息(如基因表达量、致癌基因的表达通路等)融入影像学方法,有潜力发现无侵入且生物学可解释性强的预后影像学标记物,从而促进影像学标记物在个体化医疗的应用与发展,在肿瘤疗效与预后评估、新治疗靶点和肿瘤生物机制理解方面,均具有积极意义。
中科院苏州医工所高欣、夏威、陈颖、张睿等人以肝细胞癌为实验对象,开展了影像基因组学的初步研究。该研究获取了癌症基因图谱数据库(The Cancer Genome Atlas,TCGA)上371例肝细胞癌患者基因表达数据与总生存期,及其中38例患者的增强CT数据。针对CT数据,采用基于体素的子区域聚类方法,将肿瘤区域划分为3个子区域。从各子区域中,提取了影像组学特征,并采用稳定性和冗余性分析方法筛选影像特征。针对基因表达数据,采用权重基因共表达网络分析(WGCNA),获取多个基因模块,并分析总生存期数据,得到具有生存期预测能力的预后基因模块。为了理解预后基因模块的生物学功能解释,对基因模块注释分析。通过构建影像特征与预后基因模块的Spearman秩相关矩阵,找出了与基因模块显著相关的影像特征。最后利用 Cox 比例风险回归模型,评估了这些影像特征的总生存期预测能力。
研究结果表明,8个影像组学特征与基因模块显著相关,最终确定其中2个影像组学特征有潜力作为肝细胞癌生存期预测的影像学标记物。其中,子区域体积分数 (volume fraction_2),与代表癌症相关通路的6个基因模块均显著相关,且该影像特征与肝细胞癌患者的总生存期(P =0.022,风险比=0.24)显著相关;描述肿瘤子区域异质性的纹理特征集群突出 (cluster prominence_3),与代表脂肪代谢和补体活动的基因模块显著相关,且也与总生存期(P=0.021,风险比=0.17)显著相关。
相关研究结果发表在Physics in Medicine and Biology (SCI IF 2.742):
Wei Xia, Ying Chen, Rui Zhang, Zhuangzhi Yan, Xiaobo Zhou, Bo Zhang, Xin Gao*, Radiogenomics of Hepatocellular Carcinoma: Multiregion Analysis-Based Identification of Prognostic Imaging Biomarkers by Integrating Gene Data——A Preliminary Study, Physics in Medicine and Biology, 2018, 63(3). 文章链接:http://iopscience.iop.org/article/10.1088/1361-6560/aaa609/meta
该研究工作得到了国家自然科学基金(81571772)等项目资助。
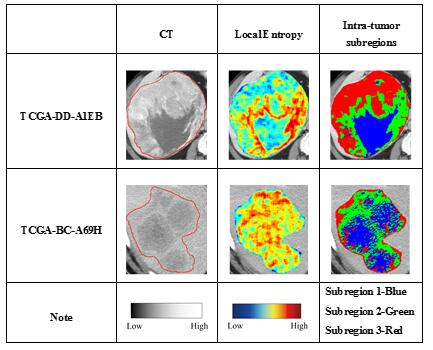
图1. 肿瘤增强CT图像子区域聚类分割结果, 第一列是原始 CT图像,第二列是肿瘤区域局部熵特征热图,第三列是生成的3个不同颜色代表的子区域。
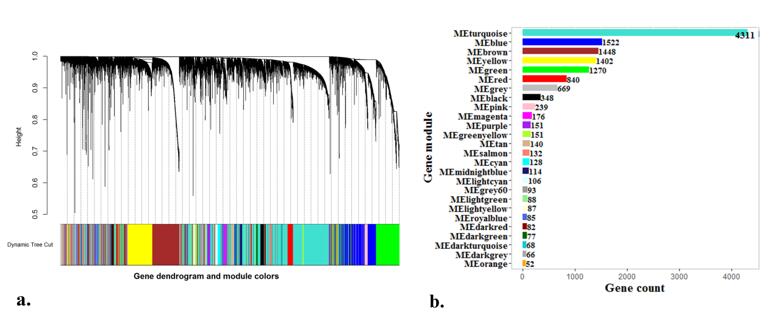
图 2. 采用WGCNA方法获得的基因聚类树状图及基因模块。(a)基因树状图,每种颜色表示一个基因模块;(b)每个基因模块中基因的数量。
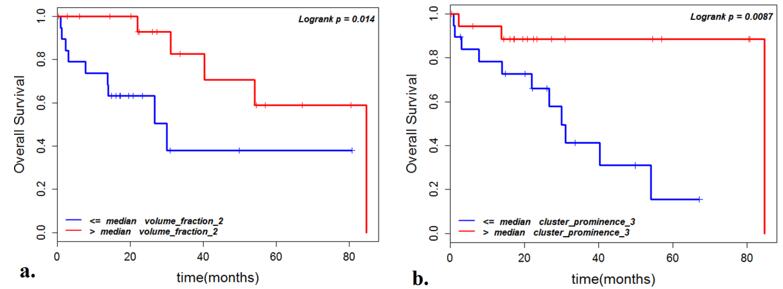
图3. Kaplan-Meier生存分析曲线图。(a)与(b)分别显示了影像特征 “volume fraction_2”与“cluster prominence_3”对总生存期的预测能力。可以看出影像特征值较大的患者生存率较高(红线),反之则生存率较低(蓝线)。
 附件下载:
附件下载: