新华网最新报道指出每年新发癌症病例约380万,死亡人数约229万,总体癌症发病率平均每年上升3.9%左右,发病率及死亡率呈现逐年上升趋势。目前,治疗癌症的主要手段有手术切除、放疗、化疗和分子靶向药物等。其中手术和放疗为局部治疗,化疗和分子靶向药物治疗为全身治疗。另外还有内分泌治疗、生物治疗等。一些微创治疗方法,如介入治疗、电化学治疗、激光治疗、微波热疗、超声热疗、冷冻治疗、射频治疗等有时也能取得治疗效果。
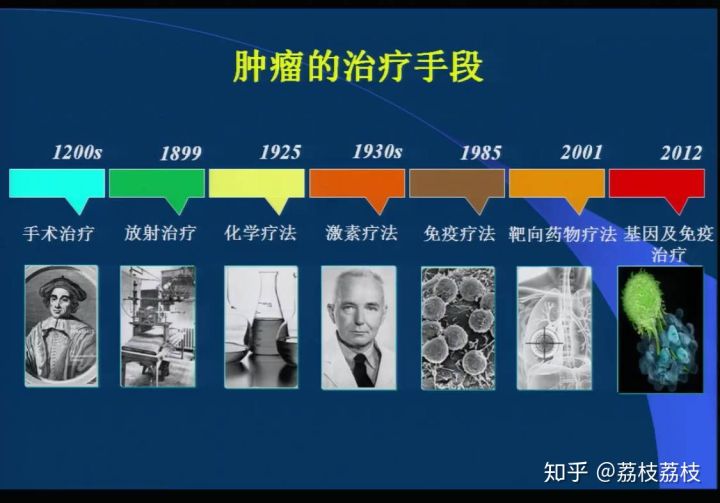
面对不同的治疗方法,癌症患者应该如何选择?
可根据肿瘤的不同性质选择不同的治疗方法,肿瘤的发现时间、恶性程度等也都能影响其治疗方式的选择。如果有长期的慢性疾病病史或者肿瘤家族史的病人,应该做好定期的监测。如果肿瘤检测物检测结果升高,要进一步的完善影像学等方面的检查,明确是否存在肿瘤的可能。单纯的肿瘤标记物检测升高不一定就是肿瘤,还可能受到其他方面的因素影响,做到早检查、早发现、早治疗可以大大增加治愈的可能性。
何为肿瘤标志物?
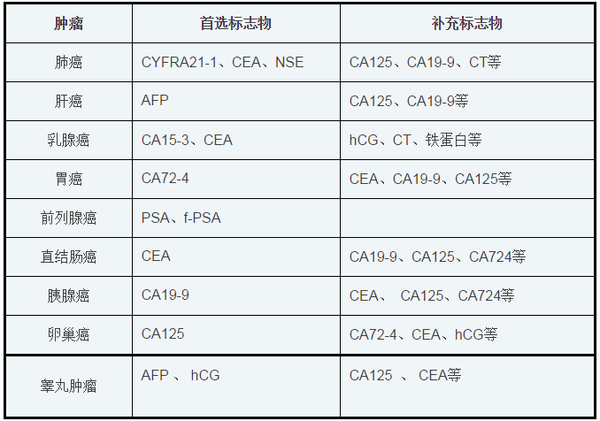
肿瘤标志物是指特征性存在于恶性肿瘤细胞,或由恶性肿瘤细胞异常产生的物质,或是宿主对肿瘤的刺激反应而产生的物质,并能反映肿瘤发生、发展,监测肿瘤对治疗反应的一类物质。肿瘤标志物存在于肿瘤患者的组织、体液和排泄物中,能够用免疫学、生物学及化学的方法检测到。例如,癌胚抗原(CEA)和甲胎蛋白(AFP)是两种常见的肿瘤标志物。CEA在胃肠道肿瘤、肺癌、乳腺癌中可出现异常增高,AFP在肝癌和恶性畸胎瘤中可出现异常增高。研究人员发现,血清中CEA和AFP的浓度与多种癌症的发生发展有关,同时检测这两种蛋白在癌症的诊断中具有重要作用。
检测方法有哪些?
肿瘤标记物的检测主要是针对于肿瘤生长过程当中产生的小分子的物质,如果浓度异常的升高,高度提示肿瘤的可能。如从血清学水平检测肿瘤标记物,需要抽血进行相关指标的检查。使用放射免疫分析和酶联免疫分析,以及全自动免疫化学分析系统,来定量检测肿瘤标志物,使用免疫组化或原位分子杂交组化技术等,检测组织中的肿瘤标志物。肿瘤是临床常见的一大类疾病,对于肿瘤的检测,大多数需要进行综合性的评估。
检测方法新进展
目前,常规的检测方法包括酶联免疫吸附试验(ELISA)和化学发光免疫分析(CLIA)等,但现有方法存在发光强度低、成本高、不易测量等缺点。为满足现有临床诊断对于分析测试方法提出的越来越高的要求,需要建立一种更为方便、稳定和灵敏的分析方法,用于在癌症的早期诊断中同时检测多种肿瘤标志物分子。
银纳米簇(AgNCs)由几个到几十个银原子组成,它们的超小尺寸接近电子的费米波长,从而其连续的能带被分离成多个独立的能级,展示出许多类分子特性如强荧光性,可作为一种荧光信号源用于生物分子检测。以DNA为模板合成的银纳米簇往往具有较高的荧光量子产率,高光稳定性,可调荧光发射和良好的生物相容性等优点,可以作为一种新型免标记荧光探针用于化学传感和生物医学检测领域。
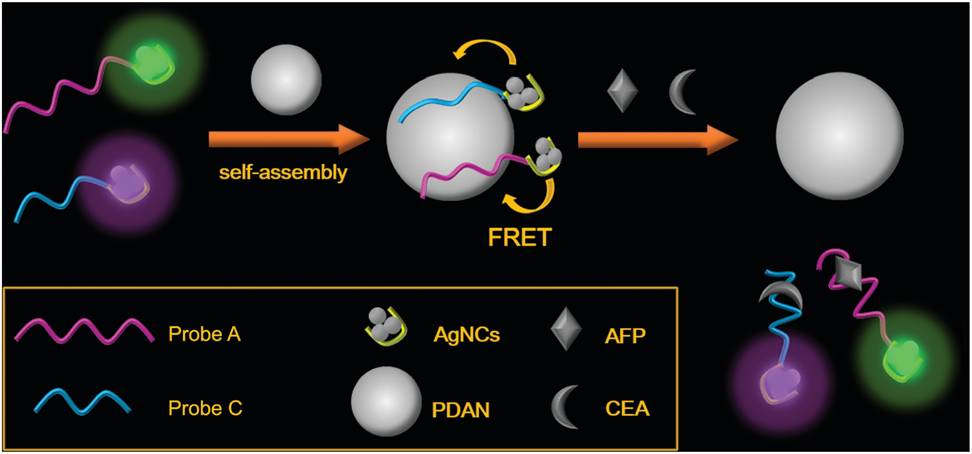
近期,中科院苏州医工所缪鹏研究员课题组提出了一种新型的基于银纳米簇的荧光检测方法,用于同时检测AFP与CEA。相应的研究成果已发表(Nanoscale, 2019, 11, 8119)。该项工作中,首先引入聚多巴胺纳米球@银纳米簇(PDAN@AgNCs)体系,并使用不同的DNA模板合成具有不同荧光发射性质的银纳米簇,模版的另一端分别包含针对不同肿瘤标志物的适配体序列。单链DNA序列可以通过π-π堆积吸附在聚多巴胺纳米球的表面上导致银纳米簇的荧光猝灭。在存在相应的肿瘤标志物时,形成的适配体/靶标蛋白复合物可以从聚多巴胺纳米球的表面释放出来,游离的银纳米簇发射的荧光信号可用于指示相应肿瘤标志物的浓度。随着肿瘤标志物浓度的提高,相应的荧光发射变强,其浓度与荧光强度呈正相关。原理图如下:
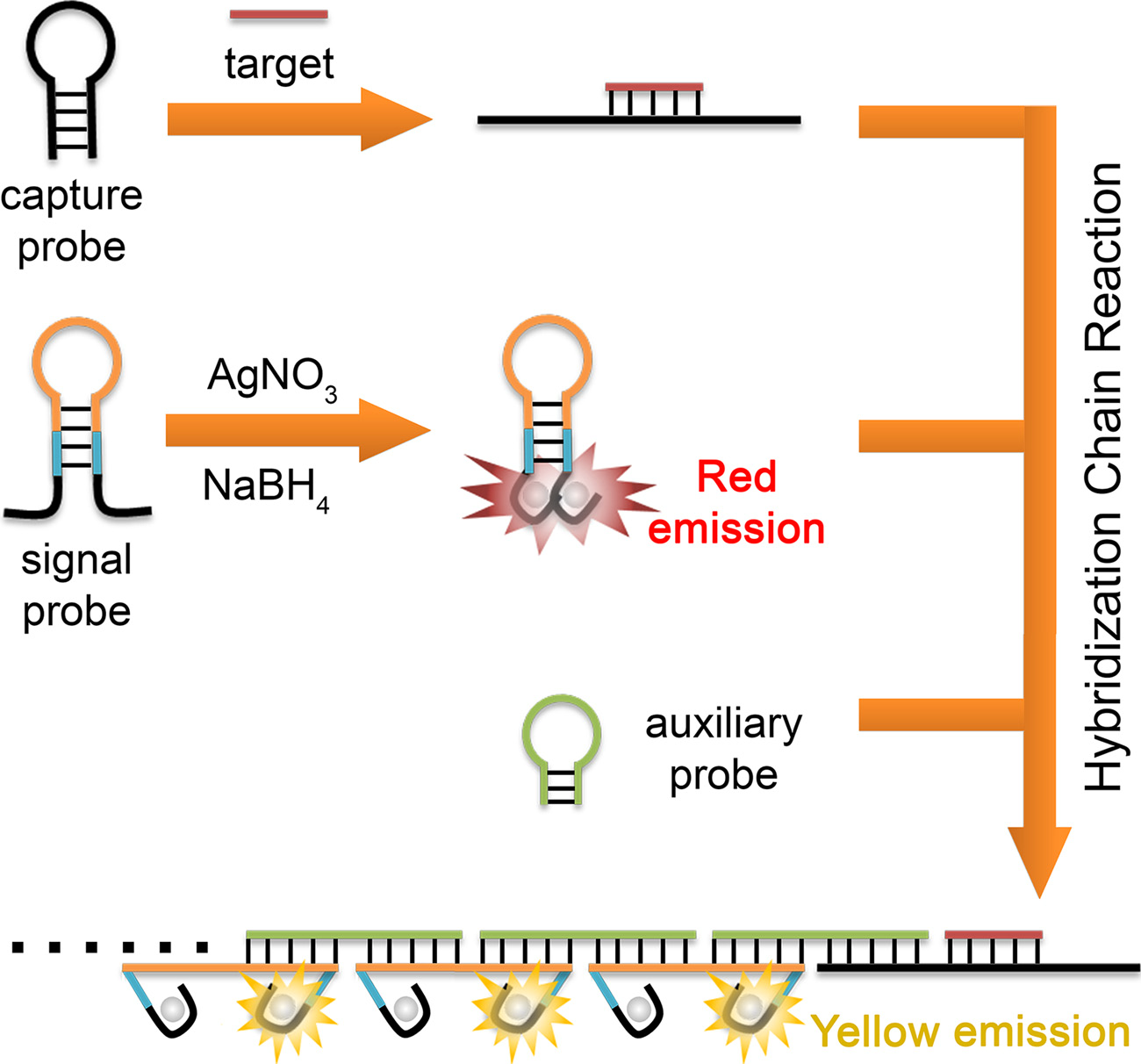
miRNA是一类非编码小分子RNA,是基因表达的关键调节因子。越来越多的报道指出miRNA在调节细胞分化、增殖和凋亡中起到关键作用,其异常表达往往发生在病理细胞中。此外,由于miRNA与其他长链RNA相比非常稳定,因此它们被认为是诊断多种疾病的理想标志物。在前期银纳米簇的研究基础上,该课题组进一步研发了一种基于银纳米簇荧光调控的比率型miRNA传感策略,并引入了杂交链式反应,在目标miRNA存在条件下,将原有的红色荧光转变成黄色荧光,不仅保证了高灵敏度的检测,还可用于miRNA在细胞内的原位成像。该传感策略还将信号生成与放大组合为一个步骤,极大地简化了程序并缩短了检测时间。所合成的银纳米簇是以DNA为模板,具有较高的荧光量子产率,光稳定性,可调荧光发射和良好的生物相容性等,有望广泛应用于光学传感和生物医学成像。相应的研究成果已发表(Sensors & Actuators: B. Chemical, 2019, 297, 126788)。
原理图如下:
 附件下载:
附件下载: